
提示
解锁ADC药物质控密码!月旭HIC色谱柱闪耀登场
2025-04-02
生物大分子药物近年来发展迅猛,特别是以抗体药物偶联物(Antibody drug conjugate,生物分子药物近年来发展迅猛,特别是以抗体药物偶联物(Antibody drug conjugate,ADC)为代表的新型药物正以惊人的速度崛起,成为肿瘤治疗领域中一颗璀璨的新星。ADC是通过连接子将抗体与细胞毒性载药偶联而成的药物分子。
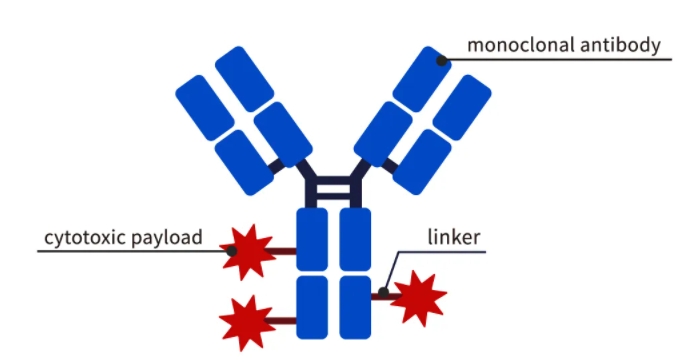
精妙绝伦的设计,使ADC兼具抗体药物精准靶向性和小分子细胞毒性药物高效杀伤的双重优势,犹如一枚精准制导的 “生物导弹”,在肿瘤的靶向治疗中发挥着重要作用。截止目前,全球已有17款ADC药物被批准上市。其中,仅2024年就有83种新的ADC首次进入临床。据不完全统计,全球ADC药物市场规模已超过130亿美元。
ADC作为生物治疗药物本身结构复杂,且具有高度非均一性的特点,给其质控增加了难度,对分析检测方法提出了更加严苛的要求。其中,药物抗体比(Drug-to-antibody ratio, DAR)不仅直接反映靶向肿瘤细胞的载荷数量,同时影响ADC药物的治疗效果和安全性。因此,在ADC开发过程和商业化生产运营中,作为关键质量属性之一的DAR的测定和监测尤为重要。
疏水色谱(Hydrophobic Interaction Chromatography,HIC)是一种利用分析样品的疏水性差异进行分离的色谱模式,常用于ADC药物的DAR评估。
为此,我们月旭科技推出了一款基于疏水作用机理的高性能蛋白分离色谱柱Advanchrom HIC-Butyl,它采用先进的大孔硅胶微球为基质,结合独特的表面键合技术,适用于抗体以及ADC的分离表征。

01 产品特点
● 独特的化学设计,对抗体偶联药物分子(ADC)具有良好的选择性
● 超高纯大孔硅胶微球基质,柱效高
● 非特异性吸附低,回收率高
● 耐压及耐受性好
● 批次间一致性佳
● 使用较低的盐组分即可获得样品良好的保留与分离
02 产品信息

03 案例分析
应用案例1:双抗ADC的DAR分析
色谱条件:
色谱柱:Advanchrom HIC-Butyl
规格:3 μm, 4.6 × 50 mm
流动相:
A)100 mM磷酸钠缓冲溶液+1.0 M硫酸铵, pH 7.0
B)100 mM磷酸钠缓冲溶液, pH 7.0/异丙醇=80/20
洗脱程序:
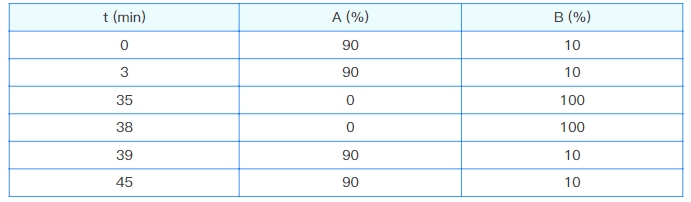
流速:0.5 mL/min
检测波长:280 nm
柱温:25 ℃
进样量:10 μL
样品:ADC
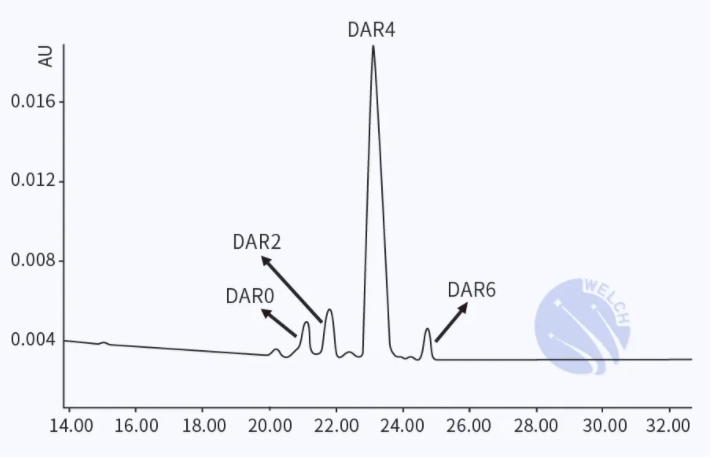
图1 双抗ADC样品不同DAR分布
结论:在硫酸铵体系下,具有不同DAR的ADC分子可在HIC柱上实现良好的保留与高效的分离。其中裸抗疏水性最弱,优先被洗脱,偶联小分子药物数量越多的分子,其疏水性就越强,越晚洗脱。
虽然使用硫酸铵体系作为流动相在DAR的测定中有广泛的应用,但由于其作为非挥发性盐,不能实现与MS的兼容。为此我们在也尝试了乙酸铵(挥发性盐)体系,在HIC柱上获得单抗ADC药物DAR2峰(如图2)与利妥昔单抗峰(如图3)的良好保留与优异峰形,为后续DAR的MS鉴定提供可兼容的流动相体系。
应用案例2:单抗ADC的DAR2测定
色谱条件:
色谱柱:Advanchrom HIC-Butyl
规格:3 μm, 4.6 × 50 mm
流动相:
A)1.0 M乙酸铵
B)25 mM乙酸铵/乙腈=70/30
洗脱程序:

流速:0.5 mL/min
检测波长:280 nm
柱温:30 ℃
进样量:10 μL
样品:ADC
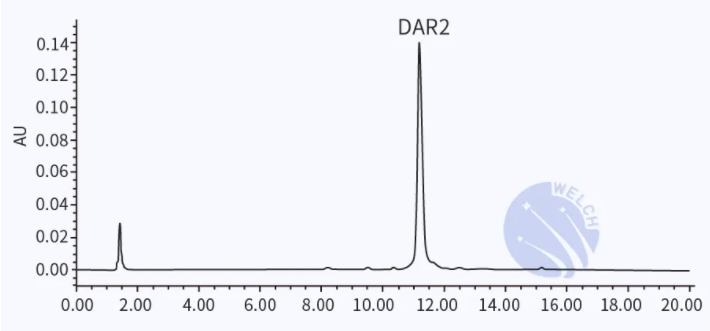
图2 单抗偶联ADC样品DAR2
应用案例3:完整抗体(利妥昔单抗)的测定
色谱条件同案例2
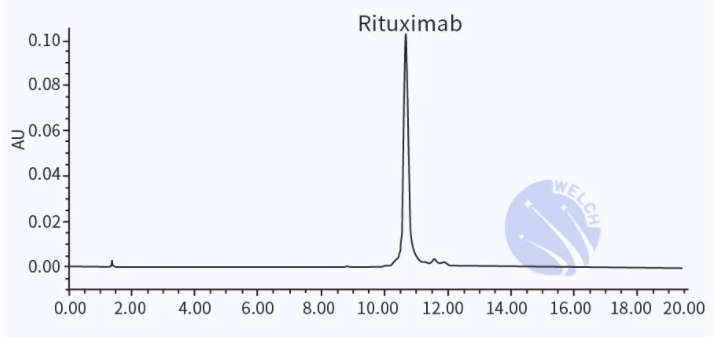
图3 利妥昔单抗样品
应用案例4:标准蛋白的分离
色谱条件:
色谱柱:Advanchrom HIC-Butyl
规格:3 μm, 4.6 × 50 mm;3 μm, 4.6 × 35 mm
流动相:
A)100 mM磷酸钠缓冲溶液+2.0 M硫酸铵, pH 7.0
B)100 mM磷酸钠缓冲溶液, pH 7.0/乙腈=90/10
洗脱程序:

流速:1.0 mL/min
检测波长:280 nm
柱温:30 ℃
进样量:10 μL
样品:(~1 mg/mL溶于流动相A中)
1. 核糖核酸酶A 2. 溶菌酶 3. α-胰凝乳蛋白酶原

图4 标准蛋白的分离(对比市售HIC柱)
结论:月旭科技的两款HIC柱均可实现三种标准蛋白的良好保留与分离,且峰形与塔板数均优于某竞品柱。
04 流动相推荐
● 在HIC-UV下,硫酸铵与乙酸铵体系均可尝试以获得更为满意的实验结果。
● HIC-MS下,使用乙酸铵体系。
05 质量保证
每一根出厂的HIC-Butyl色谱柱都经过成熟的装柱工艺和严格的质量管理体系生产,以确保良好的分离性能。
06 订货信息






